#1
لافالانتينا
~{::. إداريه سابقة .::}~
بيانات العضوة
- رقم العضوية : 1337
- تاريخ التسجيل: 123Jan 2011
- الدولة : egypt
- المدينة : اليكس حاليا
- الحالة الاجتماعية : متزوجة
- الوظيفة : تربية انجليزى
- المشاركات: 60,582 [+]
- الأصدقاء : 362
- نقاط التقييم : 34
 المطر الحمضى
المطر الحمضى
محطة توليد الطاقة من الفحم في أوهايو
المطر الحمضي (بالإنجليزية: Acid rain) هو مطر أو أي نوع من الهطول يحتوي على أحماض. الأمطار الحمضية لها تأثيرات مدمرة على النباتات والحيوانات المائية. معظمها تتكون بسبب مركبات النيتروجين والكبريت الناتجة عن الأنشطة البشرية والتي تتفاعل في الجو لتكوّن الأحماض. في السنوات الأخيرة، الكثير من الحكومات وضعت قوانين للحد من هذه المركبات المسببة للأمطار الحمضية.
على البيئة البحرية
تتكون الأمطار الحمضية من تفاعل الغازات المحتوية على الكبريت. وأهمها ثاني أكسيد الكبريت مع الأكسجين بوجودالأشعة فوق البنفسجية الصادرة عن الشمس، وينتج ثالث اكسيد الكبريت الذي يتحد بعد ذلك مع بخار الماء الموجود في الجو، ليعطي حمض الكبريت.
الذي يبقى معلقا في الهواء على هيئة رذاذ دقيق تنقله الرياح من مكان لاخر، وقد يتحد مع بعض الغازات في الهواء مثل النشادر، وينتج في هذه الحالة مركب جديد هو كبريتات النشادر، اما عندما يكون الجو جافا، ولا تتوفر فرصة لسقوط الأمطار، فان رذاذ حمض الكبريت، ودقائق كبريتات النشادر يبقيان معلقين في الهواء الساكن، ويظهران على هيئة ضباب خفيف، لاسيما عندما تصبح الظروف مناسبة لسقوط الأمطار فإنهما يذوبان في ماء المطر، ويسقطان على سطح الأرض على هيئة مطر حمضي، هذا وتشترك اكاسيد النيتروجين مع اكاسيد الكبريت في تكوين الأمطار الحمضية حيث تتحول أكاسيد النيتروجين بوجود الأكسجين والأشعة فوق البنفسجية إلى حمض النيتروجين.
ويبقى هذا الحمض معلقا في الهواء الساكن، وينزل مع مياه الأمطار، مثل حمض الكبريت مكونا الأمطار الحمضية. ولابد من إبداء الملاحظتين الآتيتين في هذا المجال. الملاحظة الأولى: ان الغازات الملوثة تنتقل بواسطة التيارات الهوائية تؤكد الدراسات في اسكندنافيا ان كمية غازات الكبريت أعلى (2.0) مرة مما تطلقه مصانعها، وفي الوقت نفسه، لا تزيد كمية غازات الكبريت في اجواء بعض اقطار أوروبا الغربية، وخاصة المملكة المتحدد عن 10- 20%. وهذا يعني ان هذه الغازات الملوثة، تنتقل بواسطة التيارات الهوائية من أوروبا الغربية إلى اسكندنافيا وإنكلترا. الملاحظة الثانية: الأمطار تزداد مع الزمن، كما جاء في كتاب "التلوث مشكلة العصر" تشير الدراسات إلى ان حموضة الأمطار التي سقطت فوق السويد عام 1982 كانت أعلى بعشر مرات من حموضة الأمطار التي سقطت عام 1969، حيث لاحظ الخبراء أن نسبة حموضة مياه الأمطار زادت بشكل منذر بالخطر، أما درجة حموضة الأمطار في بريطانيا فقد وصلت إلى 4.5 في عام 1979، ووصلت في نفس العام في كندا إلى 3.8 وفرجينيا إلى 1.5، حيث كانت درجة حموضة أمطار فرجينيا تقارب درجة حموضة حمض الكبريت (أسيد البطاريات) وفي اسكتلندا، وصلت إلى 7.2 عام 1977، ووصلت في لوس أنجلس إلى 3 عام 1980. اي أكثر حموضة من الخل وعصير الليمون، ولا يقتصر التوزع الجغرافي للأمطار على البلاد الصناعية، إذ يمكن ان تنتقل الغيوم لمسافات بعيدة عن مصادر التلوث الصناعي، فتهطل أمطارا حمضية على مناطق لا علاقة لها بمصدر التلوث. ولابد من الإشارة إلى ان درجة حموضة ماء المطر النقي هي بين 5.5 - 6 اي تميل إلى الحموضة قليلا، ولم يسجل اي تأثير سلبي لهذه النسبة، حصل خلال ملايين السنين، ويمكن اعتبار ماء المطر نقيا في حدود هذه الدرجة وغير ضار بالبيئة حسب المعلومات المتوفرة.
إن زيادة حموضة الماء تعود إلى انتقال حمض الكبريت وحمض الأزوت (النيتروجين) إليها مع مياه السيول والأنهار بعد هطول الأمطار الحمضية. إضافة إلى ذلك فان الأمطار الحمضية تجرف معها عناصر معدنية مختلفة بعضها بشكل مركبات من الزئبق والرصاص والنحاس والالمنيوم، فتقتل الأحياء في البحيرات، ومن الجدير ذكره ان درجة حموضة ماء البحيرة الطبيعي تكون بين 5-6 فاذا قلت عن الرقم 5 ظهرت المشاكل البيئية، وكما أن ماء البحيرات يذيب بعض المركبات القاعدية القلوية الموجودة في صخور القاع أو تنتقل إليها مع مياه الأنهار والسيول، فتنطلق شوارد البيكربونات وشوارد أخرى تعدل حموضة الماء، وتحول دون انخفاض الرقم الهيدروجيني، ويعبر عن محتوى الماء من شوارد التعديل ب "سعة تعديل الحمض"، فاذا تدل الإحصائيات على ان عدد البحيرات التي كانت حموضتها أقل من 5 درجات في أميركا في النصف الأول من هذا القرن كان 8 بحيرات فقط، وأصبح الآن 109 بحيرات، كما أحصي في منطقة أونتاريو في كندا، أكثر من الفي بحيرة حموضة مياهها اقل من 5 درجات، وفي السويد أكثر من 20% من البحيرات تعاني من ارتفاع الحموضة، وبالتالي الخلل البيئي واضطراب الحياة فيها.
على الغابات والنباتات

الأثر الناجم عن مطر حمضي هطل على غابة في جمهورية التشيك
إن تدمير الغابات له تأثير في النظام البيئي، فمن الملاحظ أن إنتاج الغابات يشكل نحو 15% في الإنتاج الكلي للمادة العضوية على سطح الأرض، ويكفي ان نتذكر ان كمية الاخشاب التي يستعملها الإنسان في العالم تزيد عن 2.4 مليار طن في السنة، كما أن غابات الحور المزروعة في واحد كم2 تطلق 1300 طن من الأكسجين، وتمتص نحو 1640 طنا من ثاني أكسيد الكربون خلال فصل النمو الواحد. كذلك تؤثر الأمطار الحمضية في النباتات الاقتصادية ذات المحاصيل الموسمية وفي الغابات الصنوبرية، فهي تجرد الأشجار من اوراقها، وتحدث خللا في التوازن الشاردي في التربة، وبالتالي تجعل الامتصاص يضطرب في الجذور، والنتيجة تؤدي لحدوث خسارة كبيرة في المحاصيل وعلى سبيل المثال: فقد بلغت نسبة الاضرار في الاوراق بصورة ملحوظة في احراجها 34% سحابة من الغيوم تنذر بوقوع الكارثة في ألمانيا في لسبعينات وازدادت إلى 50% عام 1985.
وفي السويد وصلت الأضرار إلى 30% في احراجها، وتشير التقارير إلى ان 14% من جميع اراضي الاحراج الأوروبية قد اصابها الضرر نتيجة الأمطار الحمضية. إضافة إلى ان معظم الغابات في شرقي الولايات المتحدة الاميركية، تتأثر بالأمطار الحمضية، لدرجة ان اطلق عـلى هذه الحالة اسم فالدشترين وتعني موت الغابة، علما بان أكثر الاشجار تأثرا بالأمطار الحمضية هي الصنوبريات في المرتفعات الشاهقة.. نظرا لسقوط اوراقها قبل اوانها مما يفقد الاخشاب جودتها، وبذلك تؤدي إلى خسارة اقتصادية في تدمير الغابات وتدهورها.
على التربة
تبين التقارير ان التربة في مناطق أوروبا، اخذت تتأثر بالحموضة، مما يؤدي إلى اضرار بالغة من انخفاض نشاط البكتيريا المثبتة للنيتروجين مثلا. وانخفاض معدل تفكك الاداة العضوية، مما أدى إلى سماكة طبقة البقايا النباتية إلى الحد الذي أصبحت فيه تعوق نفاذ الماء إلى داخل التربة والى عدم تمكن البذور من الانبات، وقد ادت هذه التأثيرات إلى انخفاض إنتاجية الغابات...
على الحيوانات
تتوقف سلامة كل مكون من مكونات النظام البيئي على سلامة المكونات الأخرى، دخان المصانع السبب الرئيسي فمثلا تأثر النباتات بالأمطار الحمضية يحرم القوارض من المادة الغذائية والمأوى، ويؤدي إلى موتها أو هجرتها، كما تموت الحيوانات اللاحمة التي تتغذى على القوارض أو تهاجر أيضا وهكذا.. وقد يلاحظ التأثير المباشر للأمطار الحمضية في الحيوانات. كما لوحظ موت القشريات والاسماك الصغيرة في البحيرات المتحمضة، نظرا لتشكل مركبات سامة بتأثير الحموض (الأمطار الحمضية)، تدخل في نسيج النباتات والبلانكتون- العوالق النباتية- (نباتات وحيدة الخلية عائمة).. وعندما تتناولها القشريات والاسماك الصغيرة، تتركز المركبات السامة في انسجتها بنسبة أكبر. وهكذا تتركز المواد السامة في المستهلكات الثانوية والثالثية حتى تصبح قاتلة في السلسلة الغذائية.. ولابد من الإشارة إلى ان النظام البيئي لا يستقيم إذ ا حدث خلل في عناصره المنتجة أو المستهلكة أو المفككة وبالنتيجة يؤدي موت الغابات إلى موت الكثير من الحيوانات الصغيرة، وهجرة الكبيرة منها.. وهكذا.
على الإنسان
يتشكل الضباب الدخاني في المدن الكبيرة، وهو يحتوي على حموض، حيث يبقى معلقا في الجو عدة أيام، وذلك عندما تتعرض الملوثات الناتجة عن وسائل النقل بصورة فادحة إلى الأشعة فوق البنفسجية الآتية من الشمس، فيحدث بين مكوناتها تفاعلات كيميائية، تؤدي إلى تكوين الضباب الدخاني الذي يخيم على المدن وخاصة في ساعات الصباح الأولى، والأخطر في ذلك، هو غازي ثاني أكسيد النيتروجين، لأنه يشكل المفتاح الذي يدخل في سلسلة التفاعلات الكيميائية الضوئية التي ينتج عنها الضباب الدخاني وبالتالي نكون أمام مركبات عديدة لها تأثيرات ضارة على الإنسان إذ تسبب احتقان الأغشية المخاطية وتهيجها والسعال والاختناق وتلف الأنسجة وانخفاض معدل التمثيل الضوئي في النبات الأخضر. وكل هذا ينتج عن حدوث ظاهرة الانقلاب الحراري، كما حدث في مدينة لندن عام 1952 عندما خيم الضباب الدخاني لمدة ثلاثة أيام، مات بسببه 4000 شخص، وكذلك ما حدث في أنقرة وأثينا.

أثر مطر حمضي على تمثال
آثار أخرى
الأمطار الحمضية يمكن أيضا أن تحدث أضرار ببعض أنواع المباني والآثار التاريخية والتماثيل. هذا يحدث عندما يتفاعل حمض الكبريتيك في تلك الأمطار مع مركبات الكالسيوم في الحجارة (كالأحجار الجيرية أو الرخام أو الغرانيت) لتكوين الجص الذي يتشقق ويسقط. المعادلة الكيميائية للتفاعل:
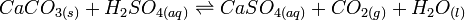
يمكن أيضا أن يتفاعل حمض الأزوت (النيتروجين) الموجود في الأمطار الحمضية مع كثير من المعادن في المنشآت الصناعية ويتسبب في تخريبها.
المطر الحمضي
نستطيع القول بأن *المطر الحمضى*مصطلح عام يطلق على الطرق العديدة التى تسقط بها الأحماض من الغلاف الجوى، والمصطلح الأكثر دقة له هو **الترسيب الحمضى** والذى يتكون من جزئين:1- ترسيب حمضي رطب wet
2- ترسيب حمضي جاف dty
2- ترسيب حمضي جاف dty
ويشير الترسيب الرطب إلى المطر الحمضى والضباب والثلج. وبما أن الماء الحمضى يتدفق فوق ومن خلال سطح الأرض فهو يؤثر على العديد من النباتات والحيوانات ومدى قوة تأثيره يعتمد على العديد من العوامل بما فيها درجة حمضية الماء، كيمياء التربة، نوع الأسماك والأشجار، وكافة الأحياء الأخرى التى تعتمد على الماء.
أما الترسيب الجاف فيشير إلى الغازات الحمضية والجسيمات.
وحوالى نصف الحمضية فى الغلاف الجوى تصل للأرض من خلال هذه الرواسب الجافة. ثم تقوم الرياح بدورها بحمل هذه الجسيمات الحمضية والغازات وترسيبها على المبانى والسيارات والمنازل والأشجار وبعدها تأتى الأمطار لتغسل هذه الأسطح من أية غازات أو جسيمات تعلق عليها بفعل الرياح، ومن هنا تتحول الأمطار إلى *أمطار حمضية*بدرجة اكبر من التى تكون عليها الأمطار عندما تتساقط فى البداية بدون أية مؤثرات خارجية.
وحوالى نصف الحمضية فى الغلاف الجوى تصل للأرض من خلال هذه الرواسب الجافة. ثم تقوم الرياح بدورها بحمل هذه الجسيمات الحمضية والغازات وترسيبها على المبانى والسيارات والمنازل والأشجار وبعدها تأتى الأمطار لتغسل هذه الأسطح من أية غازات أو جسيمات تعلق عليها بفعل الرياح، ومن هنا تتحول الأمطار إلى *أمطار حمضية*بدرجة اكبر من التى تكون عليها الأمطار عندما تتساقط فى البداية بدون أية مؤثرات خارجية.
- كيف يمكن قياس *المطر الحمضى* (حمضية المطر)؟
- تقاس *حمضية المطر* باستخدام (pH) كلما كانت رقم هذا المعامل أقل كلما كانت نسبة الحمضية فى المطر أعلى.
- نسبة (pH) فى الماء النقى = (7).
- المطر الطبيعى توجد به نسبة حمضية ضئيلة وذلك يرجع إلى تحلل ثانى أكسيد الكربون فيه وتصل النسبة فيه إلى (5.5).
- أما المطر الحمضى الذى توجد به مواد كيميائية بنسبة كبيرة من الممكن ان تصل النسبة إلى اقل من (4).
-الأسباب التى تؤدى إلى تكون *المطر الحمضى:* - يتكون هذا المطر بفعل الغازات التى تنحل فى ماء المطر لتكون أنواعاً مختلفة من الأحماض، ومن أنواع هذه الغازات:
1- غاز ثانى أكسيد الكبريتيد.
2- أكاسيد النيتروجين.
(هذان النوعان لهما الدور الأكبر فى تكوين المطر الحمضى)
2- أكاسيد النيتروجين.
(هذان النوعان لهما الدور الأكبر فى تكوين المطر الحمضى)
3- ثانى أكسيد الكربون.
4- الكلور.
4- الكلور.
- مثل هذه التفاعلات ,توضح كيفية تكون مثل هذا النوع من الأمطار:
- تفاعل ثانى أكسيد الكبريتيد مع الماء ليكون حمض الكبريتيك.
- تفاعل أكاسيد النيتروجين مع الماء لتكون حمض النيتريك.
- تفاعل ثانى أكسيد الكربون مع الماء ليكون الحامض الكربونى.
- تفاعل الكلور مع الماء ليكون حمض الهيدروكلوريك.
أمنية البوق""الثانوية الثانية ببريدة المصدر"كتاب الكيمياء في خدمة الإنسان
- مشاركات لافالانتينا
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 60,582
- لافالانتينا
- مشاهدة ملفه الشخصي
- إرسال رسالة خاصة إلى لافالانتينا
#2
صمت الورود
عضوة ذهبية
 رد: المطر الحمضى
رد: المطر الحمضى
الف شكر والله معلومة جديدة
إظهار التوقيع
توقيع : صمت الورود
التوقيع لا يظهر للزوار ..
- مشاركات صمت الورود
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 7,312
- مشاركات sho_sho
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 10,143
- مشاركات نسائم الصباح
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 18,970
- نسائم الصباح
- مشاهدة ملفه الشخصي
- إرسال رسالة خاصة إلى نسائم الصباح
- مشاركات zozoweza
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 21,576
#6
ام البنوتات
عضوة ذهبية
 رد: المطر الحمضى
رد: المطر الحمضى
الف شكر حبيبتي على المعلومات الجديدة
إظهار التوقيع
توقيع : ام البنوتات
التوقيع لا يظهر للزوار ..
- مشاركات ام البنوتات
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 4,337
- ام البنوتات
- مشاهدة ملفه الشخصي
- إرسال رسالة خاصة إلى ام البنوتات
- مشاركات mahee
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 10,760
- مشاركات رائعة
- عدد المواضيـع :
- عدد الـــــــردود :
- المجمــــــــــوع : 4,286
 قد تكوني مهتمة بالمواضيع التالية ايضاً
قد تكوني مهتمة بالمواضيع التالية ايضاً
|
||||
| الموضوع | كاتب الموضوع | المنتدى | مشاركات | آخر مشاركة |
| شعر عن المطر 2025- خواطر عن المطر - اشعار وصور عن المطر- تغريدات عن المطر والجو الجميل | وله | المنتدي الادبي | 3 | 01-05-2017 01:48 AM |
| كلمات جميلة عن المطر , اجمد كلام عن المطر , تعالى شوفى اجمل كلام | Marwa El-shazly | الحملات الدعوية | 4 | 23-12-2015 08:38 PM |
| كلمات جميله عن المطر , اجمل ما قيل عن المطر , اقوال جميله عن المطر | صفاء الحياة | حكم واقـوال | 10 | 22-12-2015 06:08 PM |
| آداب وأحكام المطر والرعد والبرق والريح والبَرَدَ | زاهرة الياياسمين | الحملات الدعوية | 6 | 08-12-2015 11:23 PM |
| كلام عن المطر حكم واقوال عن المطر في الشتاء | عشق2001 | حكم واقـوال | 4 | 07-09-2015 10:44 PM |
الساعة الآن 08:03 PM
جميع المشاركات تمثل وجهة نظر كاتبها وليس بالضرورة وجهة نظر الموقع

